 Пролиферативная витреоретинопатия (ПВР) - обширный спектр витреоретинальной патологии, сопровождающейся процессами патологического мембранообразования на поверхности сетчатки и в стекловидном теле, приводящего в конечном итоге к необратимым и неоперабельным изменениям. В отслоенной сетчатке, потерявшей связь с хориоидеей — основным поставщиком кислорода, развивается ацидоз. Гипоксия сетчатки увеличивает проницаемость гематоретинального барьера и способствует миграции не только клеточных элементов, но и факторов роста (митогены, фибронектины, хемокины и т. д.).
Пролиферативная витреоретинопатия (ПВР) - обширный спектр витреоретинальной патологии, сопровождающейся процессами патологического мембранообразования на поверхности сетчатки и в стекловидном теле, приводящего в конечном итоге к необратимым и неоперабельным изменениям. В отслоенной сетчатке, потерявшей связь с хориоидеей — основным поставщиком кислорода, развивается ацидоз. Гипоксия сетчатки увеличивает проницаемость гематоретинального барьера и способствует миграции не только клеточных элементов, но и факторов роста (митогены, фибронектины, хемокины и т. д.).
Теория пролиферативной витреоретинопатии
Термин «пролиферативная витреоретинопатия» стал широко использоваться с 1983 г., когда был применен для описания степени ретракционных процессов в новой классификации отслоек сетчатки. В том же году классификация была представлена и принята на заседании Американской академии офтальмологов и используется по настоящее время практически в неизменном виде (Retina Society Terminology Committee, 1983).
Классификация базируется на теории Роберта Махемера об образовании патологических коллагеновых структур (мембран) на поверхности сетчатки и стекловидного тела, вызывающих ретракцию. Роберт Махемер так описывает процессы образования мембран, которые он первоначально называл массивной периретинальной ретракцией: после образования разрыва сетчатки клетки ретинального пигментного эпителия (РПЭ) покидают свое нормальное местоположение, распространяются в субретинальном и интравитреальном пространстве, трансформируются в клетки, производящие коллаген, оседают на поверхности стекловидного тела и на поверхности сетчатки; умножаются в результате деления и производят патологический коллаген, который собственно и приводит к ретракции. Кроме того, в формировании эпиретинальных мембран принимают участие глиальные клетки, которые выходят из сетчатки на ее поверхность. Таким образом, образование патологических мембранных структур - результат трансформации клеток РПЭ, которые вследствие отслойки сетчатки покидают свое привычное положение, через разрыв сетчатки проникают в витреальную полость, распространяются по стекловидному телу и поверхности сетчатки и в сочетании с глиальными клетками, в свою очередь проникшими через сетчатку на ее поверхность, образуют патологические мембраны, приводящие к ретракционным процессам. Необходимо подчеркнуть, что Роберт Махемер утверждал, что процесс развития ПВР напрямую не зависит от наличия или отсутствия стекловидного тела, что патологическое мембранообразование может происходить на поверхности сетчатки после произведенной витрэктомии.
Однако теория ПВР содержит ряд сомнительных моментов, на которые необходимо обратить внимание. Вызывает сомнение, что клетки РПЭ могут трансформироваться. Возможность трансформации зависит от степени дифференциации клеток. Клетки РПЭ относятся к высокоспециализированным и, следовательно, не обладают способностью к последующей трансформации. Остается неясным, каким образом клетки РПЭ преодолевают встречный ток внутриглазной жидкости, попадая в витреальную полость. При отслойке сетчатки жидкость из витреальной полости, по пути наименьшего сопротивления, через разрыв сетчатки устремляется в субретинальное пространство, что вызывает постоянный ток жидкости, который должны преодолеть клетки РПЭ.
Без ответа остается вопрос: почему в подавляющем большинстве случаев после успешно проведенного эписклерального пломбирования проникшие в витреальную полость клетки РПЭ не вызывают никаких последствий? Почему при гигантских отрывах сетчатки от зубчатой линии в послеоперационном периоде не происходит тяжелейших пролиферативных процессов, несмотря на теоретическую возможность выхода огромного числа пигментных клеток в витреальную полость? При пошаговом рассмотрении теории ПВР и сопоставлении ее с практикой число вопросов продолжает увеличиваться. Существующая теория не позволяет объяснить происхождение эпиретинального фиброза без отслойки сетчатки. Вне логики теории ПВР остаются процессы и механизмы, приводящие к возникновению разрыва и последующей отслойки сетчатки. Логичным выглядит предположение, что все патогенетические механизмы должны существовать в системе единого патологического процесса.
В центральных отделах, непосредственно на поверхности сетчатки, обнаружен тончайший слой стекловидного тела толщиной 1,5-2 микрона. На поверхности слоя стекловидного тела располагались клетки размеры которых изменялись в зависимости от их состояния. В неактивной фазе размеры клеток составляют 3 микрона и имеют шарообразную форму, в активной - клетки приобретают звездчатую форму и увеличиваются до 90 микрон. В активной фазе видны явные признаки синтезируемого коллагена, лучи клеток звездчатой формы оканчиваются фибриллами стекловидного тела, на котором эти клетки располагаются. Это доказывает что стекловидное тело человека может синтезироваться прижизненно, т.к. часть пула клеток стекловидного тела, в частности клетки, располагающиеся у поверхности сетчатки, можно отнести к клеткам, синтезирующим нормальный коллаген стекловидного тела, - витреальным фибробластам.
Классификация
ПВР прогрессирует особенно бурно после неудачных операций. Распространяясь по сетчатке и ЗГМ, пролиферативная ткань, со временем подвергаясь фиброзу, начинает сокращаться, стягивая сетчатку в неподвижные, фиксированные складки. В результате дальнейшего фиброза складки сетчатки подтягиваются к центру, и сетчатка приобретает воронкообразную конфигурацию.
Ретинальное общество США предложило в 1983 году клиническую классификацию ПВР. В соответствии с классификацией, выделяются 4 стадии ПВР. Деление на стадии определяется по состоянию сетчатки и стекловидного тела.
- Стадия A - минимальные проявления ПВР. Сетчатка отслоена, при биомикроскопии определяются частицы пигмента в СТ, на сетчатке нет фиксированных складок
- Стадия B - умеренная ПВР. На сетчатке имеется складчатость, сосуды на складках извитые, края разрывов завернуты.
- Стадия С - выраженная ПВР. Характеризуется наличием фиксированных складок и делится на 3 подстадии: С-1, С-2 и С-3.
- С-1 - фиксированные складки распространяются в пределах трех часовых меридианов (¼ окружности).
- С-2 - фиксированные складки распространяются на шесть часовых меридианов (½ окружности).
- C-3 - ПВР с фиксированными складками сетчатки в меридианах 9-ти часов (¾ окружности).
- Стадия D или массивная ПВР - фиксированные складки сетчатки распространяются на все 4 квадранта. Стадия делится на 3 подстадии: D-1, D-2 и D-3
- D-1 - складки сетчатки, занимая 4 квадранта, сходятся к ДЗН, напоминая широкую воронку.
- D-2 - конфигурация отслойки сетчатки напоминает воронку, но более узкую, чем D-1. Складки не закрывают ДЗН.
- D-3 - воронкообразная отслойка сетчатка. Складки сужаются к центру и срастаются. ДЗН не офтальмоскопируется.
Эта классификация учитывает только изменения в заднем отделе глазного яблока. Но очень часто ПВР наблюдается не только в ЗГМ, пролиферативный процесс в которой и определяет, в основном, деление на стадии, но и пролиферацию в ПГМ, у основания СТ и даже на задних волокнах цинновой связки.
Передняя пролиферативная витреоретинопатия (ППВР) развивается на крайней периферии сетчатки в области основания СТ в виде круговой мембраны, которая, начинаясь от цилиарного тела и задней поверхности радужки, прикрепляется к сетчатке позади зубчатой линии. Эта мембрана образуется в результате пролиферативного роста клеток, осевших на ПГМ и задние зонулярные волокна хрусталика. Сокращаясь в результате фиброза, мембрана начинает подтягивать сетчатку вперед. В силу этих тракций формируется круговая складка преэкваториальной сетчатки. Особенно часто ППВР встречается при афакии и артифакии.
Новая классификация ПВР, которая учитыввает локализацию пролиферативных изменений кпереди от экватара, была предложена в 1991 году R. Machemer (таб. 1). На практике эта классификация используется редко. В ней выделяют 3 стадии. Стадии А и В соответствуют классификации 1983 года. Стадия С в зависимости от расположения пролиферативных изменений относительно экватора разделяется на передний (anterior – СА) и задний (posterior – СР) типы. СР 1-12 означает, что патологические изменения расположены кзади от экватора. При СА 1-12 пролиферативный процесс развивается кпереди от экваториальной зоны. Цифры 1-12 означают количество секторов (в часах), вовлеченных в ПВР. К патологическим изменениям относят формирование фокальных, диффузных или круговых фиксированных складок сетчатки, субретинальных тяжей.
Таблица 1. Классификация ПВР по R. Machemer
|
Стадия |
Клинические проявления |
|
А |
Стекловидное тело мутное, с включениями пигмента. Пигмент на поверхности отслоенной сетчатки в нижних отделах витреальной полости |
|
B |
Сморщивание поверхности отслоенной сетчатки, уменьшение ее подвижности; ретинальные сосуды извиты; края разрыва сетчатки завернуты; стекловидное тело становится малоподвижным |
|
C posterior (1-12) |
Кзади от экватора формируются фокальные, диффузные фиксированные складки сетчатки; наличие субретинальных тяжей |
|
C anterior (1-12) |
Кпереди от экватора формируются фиксированные складки сетчатки; переднее смещение сетчатки; плотное тяжистое стекловидное тело |
Лечение
В настоящее время хирургическим «золотым стандартом» при ПВР является витрэктомия и удалением эпиретинальных мембран вне зависимости от стадии процесса.
Массивная преретинальная пролиферация не является противопоказанием к проведению операции. При воронкообразных отслойках сетчатки, при ПВР в стадии D-2 и D-3 операции возможны и должны проводиться, если процесс двухсторонний, или если это единственный глаз, или если сохранено уверенное светоощущение. Выраженная субретинальная плакоидная (пластинчатая) пролиферация может быть противопоказанием к проведению операции особенно, если второй глаз функционирует. То же самое относится к глазам, которые были несколько раз оперированы безуспешно, особенно если уже несколько раз проводились трансвитреальные операции (витрэктомия, мембранопилинг, введение силикона и т. д.). Значительная гипотония и начавшаяся субатрофия глазного яблока не являются противопоказанием к операции.
От операции следует воздержаться в случаях выраженных воспалительных изменений. В таких случаях необходимо провести активное противовоспалительное лечение.
Хирургическая техника
Неэффективные пломбы, наложенные недавно (до одного месяца), следует удалять. Если рецидив отслойки сетчатки возник через несколько месяцев после успешной операции пломбирования, удаление пломбы нецелесообразно. При катарактальных изменениях хрусталика его следует удалить. Предпочтительнее имплантировать ИОЛ с фиксацией в капсульный мешок. Сохранение капсульного мешка и имплантация ИОЛ необходимы, так как в ряде случаев требуется длительная тампонада полости СТ силиконовым маслом, и в случае бескапсульной афакии возможен нежелательный выход силикона в переднюю камеру и его контакт с роговицей. По этой же причине следует сохранять ранее имплантированные ИОЛ. Конечно, сохранение капсулы хрусталика и ИОЛ затрудняют визуальный контроль за ходом операции на периферии. Однако применение панорамной оптики и эндоиллюминации, а также использование эндоскопии позволяют устранить этот недостаток.
Операции при ПВР проводятся через 3 порта. Если планируется широкая эндолазеркоагуляция, то порты для введения инструментов следует располагать в диаметрально противоположных меридианах (на 3х и 9ти часах). Главным условием мобилизации отслоенной сетчатки является удаление гиалоидной мембраны. Для этого введенный через порт в СТ витреотом продвигается к заднему полюсу глаза и с его помощью осуществляется поиск отслоенного участка ЗГМ.
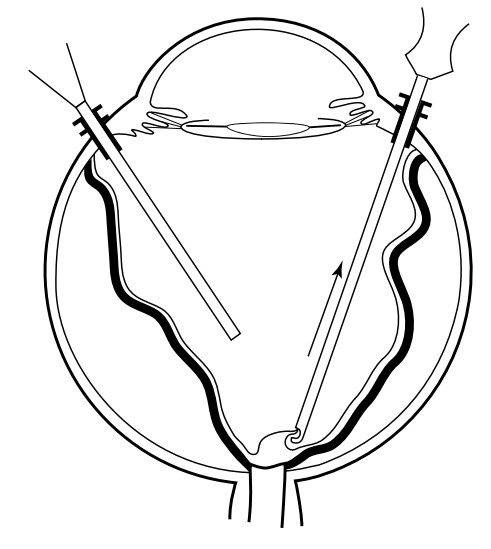 При включении режима аспирации без реза, ЗГМ втягивается в рабочее окно витреотома, и начинается ее подъем и отделение от сетчатки. Если имеются участки плотной фиксации ЗГМ с сетчаткой и она начинает двигаться, натяжение прекращается, и включается режим реза. При этом в ЗГМ образуется отверстие. Через это отверстие с помощью длинной инфузионной канюли с силиконовым наконечником производится гидроделаминация ЗГМ физиологическим раствором. Для предупреждения резкого подъема ВГД в результате активного введения физиологического раствора, подача инфузионной жидкости временно прекращается и открывается свободный отток из полости СТ. После этого через это же отверстие под ЗГМ вводится некоторое количество перфторорганического соединения (ПФОС), которое за счет своей тяжести обеспечивает фиксацию сетчатки, тем самым значительно снижая риск повреждения сетчатки в процессе выделения ЗГМ. Кроме того, с помощью ПФОС продолжается деликатная гидропрепаровка ЗГМ от сетчатки. В основе этого процесса лежат механизмы, направленные, с одной стороны, на прижатие сетчатки к оболочкам глаза за счет силы тяжести ПФОС, с другой стороны, образованный силами поверхностного натяжения округлый край ПФОС по мере его увеличения отслаивает ЗГМ от сетчатки. При необходимости для выделения периферических отделов ЗГМ можно воспользоваться тракционным воздействием с помощью выдвигаемого шпателя. Инструмент проводится через порт и выдвигается внутри глаза, принимая изогнутую форму, и его можно использовать для
При включении режима аспирации без реза, ЗГМ втягивается в рабочее окно витреотома, и начинается ее подъем и отделение от сетчатки. Если имеются участки плотной фиксации ЗГМ с сетчаткой и она начинает двигаться, натяжение прекращается, и включается режим реза. При этом в ЗГМ образуется отверстие. Через это отверстие с помощью длинной инфузионной канюли с силиконовым наконечником производится гидроделаминация ЗГМ физиологическим раствором. Для предупреждения резкого подъема ВГД в результате активного введения физиологического раствора, подача инфузионной жидкости временно прекращается и открывается свободный отток из полости СТ. После этого через это же отверстие под ЗГМ вводится некоторое количество перфторорганического соединения (ПФОС), которое за счет своей тяжести обеспечивает фиксацию сетчатки, тем самым значительно снижая риск повреждения сетчатки в процессе выделения ЗГМ. Кроме того, с помощью ПФОС продолжается деликатная гидропрепаровка ЗГМ от сетчатки. В основе этого процесса лежат механизмы, направленные, с одной стороны, на прижатие сетчатки к оболочкам глаза за счет силы тяжести ПФОС, с другой стороны, образованный силами поверхностного натяжения округлый край ПФОС по мере его увеличения отслаивает ЗГМ от сетчатки. При необходимости для выделения периферических отделов ЗГМ можно воспользоваться тракционным воздействием с помощью выдвигаемого шпателя. Инструмент проводится через порт и выдвигается внутри глаза, принимая изогнутую форму, и его можно использовать для 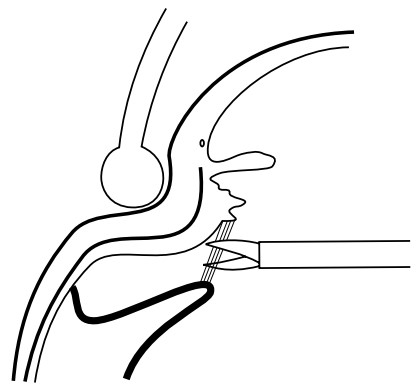 отделения ЗГМ от сетчатки. Выделенный таким образом гиалоид с остатками СТ удаляется витреотомом.
отделения ЗГМ от сетчатки. Выделенный таким образом гиалоид с остатками СТ удаляется витреотомом.
С помощью витреотома можно удалить все структуры из полости СТ, если они не прилежат непосредственно к сетчатке и не спаяны с ней. Опасность травмировать сетчатку на первых этапах невелика, так как она фиксирована преретинальными мембранами и не сдвигается при аспирации. Трудности могут возникнуть при рассечении и удалении передних петель, формирующих круговую складку сетчатки. Мембрана, образовавшаяся в результате передней пролиферации, может быть рассечена по кругу с помощью витреальных ножниц или иссечена витреотомом. Рассечение передних петель необходимо проводить под визуальным контролем с использованием бесконтактной широкоугольной оптики и склеральной компрессии.
В ходе удаления кортикальных слоев СТ, гиалоидной мембраны, эпиретинальных пленок полезно для улучшения визуализации использовать введение в полость СТ «красителя» в виде суспензий (гидрокортизон, кеналог). После введения 0,2-0,4 мл суспензии для равномерного распределения частиц необходимо создать турбулентный поток жидкости, включив инфузию и открыв один или два порта. После этого порты закрываются, и нужно выждать 1 минуту, чтобы частицы суспензии осели на остаточных структурах СТ.
Удаление эпиретинальных мембран методом мембранопилинга возможно только, если между мембраной и сетчаткой имеется лишь незначительная адгезия. В тех случаях, когда мембрана спаяна с сетчаткой очень прочно, чересчур активный пилинг может привести к разрыву сетчатки. Первым проявлением разрыва или надрыва сетчатки является кровотечение из сосудов сетчатки. Пилинг нельзя начинать от центра мембраны. Следует найти край и, захватив его пинцетом, начинать отделение мембраны, двигаясь параллельно сетчатке по направлению к центру мембраны. При этом сначала формируется складка мембраны, которая по мере расширения превращается в дупликатуру. При широкой мембране дупликатуру целесообразно формировать с разных сторон, постепенно приближаясь к центру. Полностью отделенную от сетчатки мембрану удаляют витреотомом. Если мембрана прочно сращена с сетчаткой, необходимо провести ее фрагментацию с помощью ретинальных ножниц. Особенно легко можно проводить такие разрезы между складками сетчатки. Те сегменты, которые плотно сращены с сетчаткой, удалять не следует из-за риска разрыва сетчатки.
В первую очередь необходимо освободить от мембран центральную часть сетчатки. После того, как ликвидированы грубые тракции на сетчатку вокруг ДЗН и в зоне сосудистых аркад, необходимо ввести жидкое ПФОС. Под действием ПФОС освобожденная от тракций сетчатка расправляется и прижимается к хориоидее. При введении ПФОС во избежание повышения ВГД вентиль двухпозиционного крана должен быть в таком положении, чтобы подача инфузионного раствора в глаз была прекращена, а путь для оттока жидкости из полости СТ открыт. Расслоение, рассечение мембран, мембранопилинг с применением ПФОС значительно облегчается. Прижимая сетчатку,ПФОС придерживает ее, делает менее подвижной, работает как «третья рука». ПФОС помогает выявить те участки сетчатки, которые еще не освобождены от тракций и не прилегают под его действием. Введение ПФОС целесообразно проводить дробно, вначале нужно ввести 0,75-1,0 мл. По мере увеличения участков, свободных от эпиретинальных мембран, нужно довести количество введенного ПФОС до 1,5-2,0 мл и вновь продолжать рассечение и удаление мембран. Дробное введение ПФОС позволяет более равномерно действовать на еще неосвобожденную сетчатку и снижает риск ее повреждения. Кроме того, частичное заполнение полости СТ ПФОС позволяет раздельно работать в двух разных средах. В среде ПФОС можно действовать пинцетом, ножницами и шпателем. Выше уровня ПФОС в среде инфузионной жидкости можно работать витреотомом, удаляя остатки СТ, отсепарованные эпиретинальные мембраны, отсеченные тяжи - все это всплывает на поверхность ПФОС.
Поэтапное введение ПФОС снижает опасность затекания этой жидкости под сетчатку через разрыв. В процессе удаления мембран на периферии необходимо следить, чтобы зона разрыва сетчатки была всегда выше уровня ПФОС. Это очень важно до тех пор, пока края разрыва натянуты в результате тракции. Если все мембраны и тяжи в зоне разрыва удалены, сетчатка становится подвижной и легко прилегает к сосудистой оболочке, риск проникновения ПФОС под сетчатку устраняется. После полного снятия всех тракций на сетчатку витреальная полость заполняется ПФОС полностью. Начинать введение нужно у ДЗН, все последующие дополнения необходимо производить внутрь уже введенного объема, чтобы избежать дробления ПФОС. Необходимо постоянно следить за тем, чтобы разрыв сетчатки (хотя бы один, если их несколько) находился выше уровня ПФОС, и чтобы через него СРЖ могла свободно уходить из-под сетчатки. Полностью удалить СРЖ таким способом можно, если разрыв расположен в непосредственной близости от зубчатой линии. Если разрыв находится на некотором расстоянии от ora serrata, всегда есть опасность оставить часть СРЖ под сетчаткой после того, как ПФОС прижмет края разрыва.
Для предупреждения этого осложнения необходимо перед введением ПФОС сделать точечную, дренажную ретинотомию непосредственно у ora serrata, используя при этом склерокомпрессию. Если планируется тампонада легким силиконом, такая ретинотомия делается вверху (меридиан 1-11 часов), а если тяжелым - внизу (5-7 часов). На край ретинотомии нужно нанести метку с помощью диатермии для того, чтобы ее можно было легче обнаружить и провести тщательную лазеркоагуляцию краев.
Эндолазеркоагуляция (ЭЛК) сетчатки проводится непосредственно после заполнения глаза ПФОС. Световод проводится через один из разрезов склеры. Прежде всего, коагуляцию необходимо сделать в области разрыва сетчатки. Коагуляты наносятся по краю разрыва в несколько рядов. Во многих случаях коагуляцию необходимо провести по всей периферии сетчатки на 360°, нанося коагуляты в 3-4 ряда. Особую осторожность нужно проявлять, проводя коагуляцию на 3-х и 9-ти часах с тем, чтобы не повредить задние длинные цилиарные артерии и нервы. Эндолазеркоагуляцию проводят также во всех местах, где были оставлены сегменты эпиретинальных мембран, где произошли кровотечения или возникли ятрогенные дефекты сетчатки. Все участки выраженной дистрофии сетчатки также должны быть окружены коагулятами. ЭЛК крайней периферии следует проводить с использованием широкоугольной приставки. Кроме того, необходимо проводить компрессию склеры для улучшения визуализации.
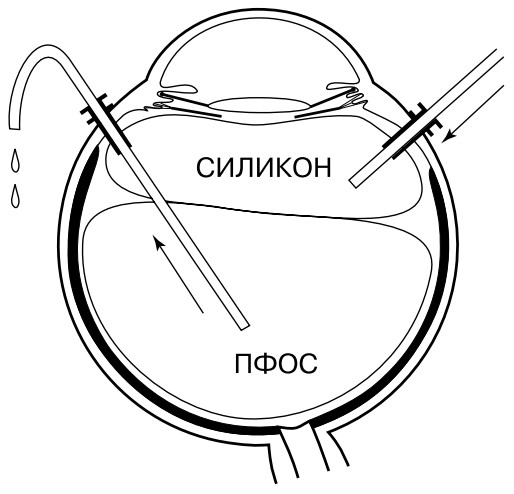 В тех случаях, когда планируется длительная тампонада полости СТ, обычно используют силиконовое масло (СМ), поэтому при завершении операции необходимо произвести еще одну замену. В полость СТ нужно ввести силикон и аспирировать ПФОС. Введение СМ производится через инфузионную канюлю, для этого она соединяется через двухпозиционный кран со шприцем, наполненным силиконом. Подача инфузионного раствора закрывается. Начиная вводить СМ, нужно помнить, что верхняя граница ПФОС расположена на уровне портов. Пространство выше этого уровня заполнено солевым раствором, который необходимо удалить. Для этого с началом введения СМ открываются оба порта, через них солевой раствор вытесняется из полости СТ. Как только в просвете порта появляется капля СМ, в него вводится инструмент. Через один порт вводится световод эндоиллюминатора, через другой - аспирационная канюля с эластичным силиконовым концом для удаления ПФОС. Одномоментную аспирацию и инъекцию нужно делать синхронно и адекватно, чтобы ВГД оставалось постоянным и находилось в пределах нормы. Надо учитывать, что силикон, имеющий большую вязкость, вводится медленно, а значительно менее вязкое ПФОС удаляется легче и быстрее. Поэтому определяющим является введение СМ, а аспирация ПФОС должна определяться скоростью введения силикона. При удалении последних капель ПФОС подачу СМ лучше отключить, остатки ПФОС эвакуируются за счет пассивной аспирации, либо при необходимости включается активная аспирация. Все это хорошо регулируется путем закрытия или открытия клапана сброса на экструзионной (аспирационной) канюле.
В тех случаях, когда планируется длительная тампонада полости СТ, обычно используют силиконовое масло (СМ), поэтому при завершении операции необходимо произвести еще одну замену. В полость СТ нужно ввести силикон и аспирировать ПФОС. Введение СМ производится через инфузионную канюлю, для этого она соединяется через двухпозиционный кран со шприцем, наполненным силиконом. Подача инфузионного раствора закрывается. Начиная вводить СМ, нужно помнить, что верхняя граница ПФОС расположена на уровне портов. Пространство выше этого уровня заполнено солевым раствором, который необходимо удалить. Для этого с началом введения СМ открываются оба порта, через них солевой раствор вытесняется из полости СТ. Как только в просвете порта появляется капля СМ, в него вводится инструмент. Через один порт вводится световод эндоиллюминатора, через другой - аспирационная канюля с эластичным силиконовым концом для удаления ПФОС. Одномоментную аспирацию и инъекцию нужно делать синхронно и адекватно, чтобы ВГД оставалось постоянным и находилось в пределах нормы. Надо учитывать, что силикон, имеющий большую вязкость, вводится медленно, а значительно менее вязкое ПФОС удаляется легче и быстрее. Поэтому определяющим является введение СМ, а аспирация ПФОС должна определяться скоростью введения силикона. При удалении последних капель ПФОС подачу СМ лучше отключить, остатки ПФОС эвакуируются за счет пассивной аспирации, либо при необходимости включается активная аспирация. Все это хорошо регулируется путем закрытия или открытия клапана сброса на экструзионной (аспирационной) канюле.
При ПВР иногда встречаются и субретинальные пролифераты, которые стягивая сетчатку, собирают ее в складки, препятствуя прилеганию. В некоторых случаях небольшие субретинальные пролифераты можно удалить либо через разрыв сетчатки, если он расположен недалеко от пролиферата, либо через специально сделанную ретинотомию. Большие субретинальные тяжи необходимо рассечь, чтобы снять тракции и добиться расправления складок. Рассечение субретинальных тяжей возможно или через существующий разрыв сетчатки, или через специально для этого сделанную ретинотомию. После рассечения субретинального тяжа, когда сетчатка расправится, зону ретинотомии необходимо окружить очагами лазеркоагуляции.
Витрэктомия в сочетании с мембранопилингом, сегментацией и деламинацией эпиретинальной мембраны (ЭРМ), тампонада с помощью ПФОС и силикона позволяют получать положительные результаты даже в очень тяжелых случаях. Чаще всего эти сравнительно сложные вмешательства проводятся на единственном глазу. Следует помнить, что восстановление функций находится в прямой зависимости от сроков заболевания. В запущенных случаях можно получить зрение лишь в несколько сотых или даже тысячных.

